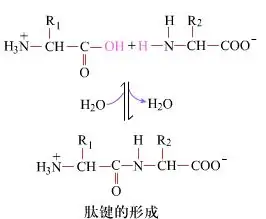
На поверхности образование пептидных связей, дающих дипептиды, является простым химическим процессом. Это означает, что два аминокислотных компонента связаны пептидной связью, амидной связью, одновременно обезвоженной.
Образование пептидной связи - это активация аминокислоты в условиях легкой реакции. (А) Карбоксильная часть, вторая аминокислота (б) нуклеофильный активированный карбоксильный фрагмент затем образует дипептид (A-B). «Если карбоксильный компонент (а) не защищен, образование пептидной связи не может контролироваться». Побочные продукты, такие как линейные и циклические пептиды, могут смешиваться с целевыми соединениями A-B. Следовательно, все функциональные группы, не участвующие в формировании пептидных связей, должны быть временно обратимым образом во время синтеза пептидов.
Таким образом, синтез пептидов - образование каждой пептидной связи - включает в себя три этапа агрегации.
Первым шагом является приготовление некоторых аминокислот, которые нуждаются в защите, а Zwitterionic Sructure аминокислот больше не существует.
Второй этап-это двухэтапная реакция с образованием пептидных связей, в которой карбоксильная группа аминокислоты, защищенной N, сначала активируется в активное промежуточное соединение, а затем образуется пептидная связь. Эта связанная реакция может возникнуть либо в виде одноэтапной реакции, либо как две последовательные реакции.
Третий шаг - селективное удаление или полное удаление защитного основания. Хотя все удаление может произойти только после того, как были собраны все пептидные цепи, также необходимо селективное удаление защитных групп, чтобы продолжить синтез пептидов.
Потому что 10 аминокислот (Ser, Thr, Tyr, ASP, Glu, Lys, Arg, His, Sec и Cys) содержат функциональные группы боковой цепи, которые требуют селективной защиты, что делает синтез пептидов более сложным. Временные и полупостоянные базы защиты должны быть выделены из-за различных требований к селективности. На следующем этапе используются группы временной защиты, чтобы отразить временную защиту аминокислотных или карбоксильных функциональных групп. Полуподосовые защитные группы удаляются без вмешательства в уже образованные пептидные связи или аминокислотные боковые цепи, иногда во время синтеза.
«В идеале, активация карбоксильного компонента и последующее образование пептидных связей (реакции связи) должны быть быстрыми, без рацемического или образования побочных продуктов, а молярные реагенты должны применяться для достижения высоких выходов». К сожалению, ни один из методов химической связи не удовлетворяет этим требованиям, и лишь немногие подходят для практического синтеза.
Во время синтеза пептидов функциональные группы, участвующие в различных реакциях, обычно связаны с ручным центром, и является единственным исключением, и существует потенциальный риск вращения.
Последним шагом в цикле синтеза пептидов является удаление всех защитных групп. Селективное удаление защитных групп важно для расширения пептидной цепи в дополнение к требованию к полному удалению защиты при синтезе дипептида. Синтетические стратегии должны быть тщательно спланированы. В зависимости от стратегического выбора N может избирательно удалить группы защиты α-амино или карбоксила. Термин «стратегия» относится к последовательности реакций конденсации отдельных аминокислот. В целом, существует разница между постепенным синтезом и фрагментной конденсацией. Пептидный синтез (также известный как «обычный синтез») происходит в растворе. В большинстве случаев постепенное удлинение пептидной цепи может быть синтезировано только с использованием пептидной цепи для синтеза более коротких фрагментов. Чтобы синтезировать более длинные пептиды, молекулы -мишени должны быть сегментированы на соответствующие фрагменты и определить, что они могут минимизировать степень дифференцировки на конце. После того, как отдельные фрагменты постепенно собираются, целевое соединение будет соединено. Стратегия синтеза пептидов включает в себя выбор лучших и наиболее подходящих защитных фрагментов, а стратегия синтеза пептидов включает в себя выбор наиболее подходящей комбинации защитных оснований и лучший метод конъюгации фрагментов.
Время публикации: 2025-07-02