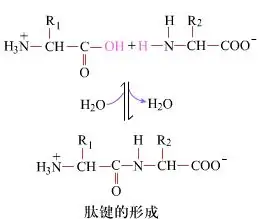
На первый взгляд образование пептидных связей, приводящих к образованию дипептидов, представляет собой простой химический процесс.Это означает, что два аминокислотных компонента связаны пептидной связью, амидной связью, в процессе дегидратации.
Образование пептидной связи — это активация аминокислоты в мягких условиях реакции.(A) карбоксильный фрагмент, вторая аминокислота (B) Нуклеофильно активированный карбоксильный фрагмент затем образует дипептид (AB).«Если карбоксильный компонент (А) не защищен, образование пептидной связи невозможно контролировать».Побочные продукты, такие как линейные и циклические пептиды, можно смешивать с целевыми соединениями АВ.Следовательно, все функциональные группы, не участвующие в образовании пептидных связей, должны быть временно обратимо защищены во время синтеза пептидов.
Итак, синтез пептидов — образование каждой пептидной связи — включает в себя три стадии агрегации.
Первым шагом является подготовка некоторых аминокислот, которые нуждаются в защите, а цвиттер-ионная структура аминокислот больше не существует.
Второй этап представляет собой двухэтапную реакцию образования пептидных связей, в которой карбоксильная группа N-защищенной аминокислоты сначала активируется до активного промежуточного продукта, а затем образуется пептидная связь.Эта связанная реакция может протекать либо как одностадийная реакция, либо как две последовательные реакции.
Третий шаг – выборочное или полное удаление защитной основы.Хотя полное удаление может произойти только после того, как все пептидные цепи собраны, для продолжения синтеза пептидов также необходимо избирательное удаление защитных групп.
Потому что 10 аминокислот (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec и Cys) содержат функциональные группы боковой цепи, которые требуют избирательной защиты, что усложняет синтез пептидов.Необходимо различать временные и полупостоянные базы защиты из-за различных требований к селективности.Временные защитные группы используются на следующем этапе, чтобы отразить временную защиту аминокислотных или карбоксильных функциональных групп.Полупостоянные защитные группы удаляются, не мешая уже образовавшимся пептидным связям или боковым цепям аминокислот, иногда во время синтеза.
«В идеале активация карбоксильного компонента и последующее образование пептидных связей (реакции сочетания) должны быть быстрыми, без образования рацемических или побочных продуктов, а для достижения высоких выходов следует применять молярные реагенты».К сожалению, ни один из методов химического сочетания не удовлетворяет этим требованиям и лишь немногие из них пригодны для практического синтеза.
При синтезе пептидов функциональные группы, участвующие в различных реакциях, обычно связаны с мануальным центром (единственным исключением является глицин), и существует потенциальный риск ротации.
Заключительным этапом цикла синтеза пептидов является удаление всех защитных групп.Селективное удаление защитных групп важно для удлинения пептидной цепи в дополнение к требованию полного удаления защиты при синтезе дипептидов.Синтетические стратегии следует тщательно планировать.В зависимости от стратегического выбора N может избирательно удалять защитные группы α-амино или карбоксила.Термин «стратегия» относится к последовательности реакций конденсации отдельных аминокислот.В общем, существует разница между постепенным синтезом и конденсацией фрагментов.Синтез пептидов (также известный как «традиционный синтез») происходит в растворе.В большинстве случаев постепенное удлинение пептидной цепи можно синтезировать только за счет использования пептидной цепи для синтеза более коротких фрагментов.Чтобы синтезировать более длинные пептиды, молекулы-мишени необходимо сегментировать на соответствующие фрагменты и определить, что они могут минимизировать степень дифференцировки на С-конце.После постепенной сборки отдельных фрагментов происходит соединение целевого соединения.Стратегия синтеза пептидов включает выбор лучшего и наиболее подходящего защитного фрагмента, а стратегия синтеза пептидов включает выбор наиболее подходящей комбинации защитных оснований и лучшего метода конъюгации фрагмента.
Время публикации: 19 июля 2023 г.